







• 研究报告 • 下一篇
收稿日期:2025-09-23
出版日期:2026-04-17
通讯作者:
祝建波,男,研究员,研究方向 :生物化学与分子生物学;E-mail: zjbshz@162.com作者简介:赵文娟,女,硕士研究生,研究方向 :植物组织培养;E-mail: 18449395133 @163.com
基金资助:
ZHAO Wen-juan, LI Hui, YANG Xue-ying, WANG Zhao-lu, ZHU Jian-bo( )
)
Received:2025-09-23
Published:2026-04-17
摘要:
目的 构建马铃薯‘新疆2号’高效再生及遗传转化体系,为抗病毒育种提供技术支撑。 方法 以‘新疆2号’马铃薯为试验材料,用农杆菌介导法将含有植物RNA干扰载体质粒pCAMBIA2300-CP-RNAi转化马铃薯茎段外植体,探究预培养时间、植物激素组合及抗生素的种类及浓度对愈伤组织诱导及芽分化的影响;通过RT-qPCR技术,以Actin基因作为内参,检测CP基因mRNA表达水平,运用酶联免疫吸附(ELISA)技术定量检测植株中PVY病毒的实际含量,验证RNAi沉默效果及病毒抑制作用。 结果 当预培养、共培养时间均为2 d时,愈伤组织诱导的最适激素和抗生素组合为2.0 mg/L 6-BA + 0.8 mg/L 2,4-D + 50 mg/L Kan + 200 mg/L TMT,诱导率为85%,愈伤组织形态紧密,为鲜绿色,茎段两端膨大呈哑铃状;茎段分化的最适激素、抗生素配比为2 mg/L 6-BA + 2 mg/L ZT + 0.5 mg/L GA3 + 50 mg/L Kan + 200 mg/L TMT时,出苗率及转化频率均达到最高,幼苗长势良好。转化苗在1/2 MS+0.6 mg/L IAA + 75 mg/L Kan + 200 mg/L TMT培养基中可形成再生植株,且根系发达。与未转化的对照植株相比,转基因植株中CP基因的相对表达量显著下调,PVY病毒的含量也明显降低,说明所构建的RNA干扰载体成功激发了特异性基因沉默效应,有效抑制了病毒在植株体内的积累。 结论 成功建立了稳定、高效的‘新疆2号’马铃薯遗传转化体系。构建的RNAi载体有效抑制了Y病毒在植株体内的积累。
赵文娟, 李辉, 杨雪莹, 王朝露, 祝建波. 马铃薯‘新疆2号’遗传转化体系的建立[J]. 生物技术通报, doi: 10.13560/j.cnki.biotech.bull.1985.2025-1016.
ZHAO Wen-juan, LI Hui, YANG Xue-ying, WANG Zhao-lu, ZHU Jian-bo. Establishment of a Genetic Transformation System for Potato ‘Xinjiang No. 2’[J]. Biotechnology Bulletin, doi: 10.13560/j.cnki.biotech.bull.1985.2025-1016.
试验编号 Test number | 6-苄氨基嘌呤 6-Benzylaminopurine(6-BA) | 2,4-二氯苯氧乙酸 2,4-Dichlorophenoxyacetic acid (2,4-D) | 萘乙酸 1-Naphthaleneacetic acid (NAA) | 3-吲哚乙酸 Indole-3-acetic acid (IAA) | 6-糠氨基嘌呤 Kinetin (KT) | 玉米素核苷 Zeatin Riboside (ZR) |
|---|---|---|---|---|---|---|
| C1 | 2.0 | 0 | 0.6 | 0 | 0 | 0 |
| C2 | 2.0 | 0.8 | 0 | 0 | 0 | 0 |
| C3 | 0 | 0 | 0 | 0.2 | 0 | 2.0 |
| C4 | 2.0 | 0.6 | 0 | 0 | 0.4 | 0 |
表1 不同激素组合对愈伤组织诱导的影响
Table 1 Effects of different hormone combinations on callus induction (mg/L)
试验编号 Test number | 6-苄氨基嘌呤 6-Benzylaminopurine(6-BA) | 2,4-二氯苯氧乙酸 2,4-Dichlorophenoxyacetic acid (2,4-D) | 萘乙酸 1-Naphthaleneacetic acid (NAA) | 3-吲哚乙酸 Indole-3-acetic acid (IAA) | 6-糠氨基嘌呤 Kinetin (KT) | 玉米素核苷 Zeatin Riboside (ZR) |
|---|---|---|---|---|---|---|
| C1 | 2.0 | 0 | 0.6 | 0 | 0 | 0 |
| C2 | 2.0 | 0.8 | 0 | 0 | 0 | 0 |
| C3 | 0 | 0 | 0 | 0.2 | 0 | 2.0 |
| C4 | 2.0 | 0.6 | 0 | 0 | 0.4 | 0 |
试验编号 Test number | 6-苄氨基嘌呤 6-Benzylaminopurine (6-BA) | 6-糠氨基嘌呤 Kinetin (KT) | 玉米素 Zeatin (ZT) | 3-吲哚乙酸 Indole-3-acetic acid (IAA) | 赤霉素 Gibberellin A₃ (GA3) | 2,4-二氯苯氧乙酸 2,4-Dichlorophenoxyacetic acid (2,4-D) |
|---|---|---|---|---|---|---|
| S1 | 2.0 | 0.2 | 1.0 | 0 | 0 | 0 |
| S2 | 2.0 | 0 | 2.0 | 0 | 1.0 | 0 |
表2 不同激素组合对愈伤组织分化的影响
Table 2 Effects of different hormone combinations on callus differentiation (mg/L)
试验编号 Test number | 6-苄氨基嘌呤 6-Benzylaminopurine (6-BA) | 6-糠氨基嘌呤 Kinetin (KT) | 玉米素 Zeatin (ZT) | 3-吲哚乙酸 Indole-3-acetic acid (IAA) | 赤霉素 Gibberellin A₃ (GA3) | 2,4-二氯苯氧乙酸 2,4-Dichlorophenoxyacetic acid (2,4-D) |
|---|---|---|---|---|---|---|
| S1 | 2.0 | 0.2 | 1.0 | 0 | 0 | 0 |
| S2 | 2.0 | 0 | 2.0 | 0 | 1.0 | 0 |
预培养时间 Pre cultivation time (d) | 外植体数 Number of explants | 愈伤数 Number of callus | 愈伤形成率 Callus formation rate (%) | 再生芽数 Number of regenerated buds | 出苗率 Seedling emergence rate (%) | 转化频率 Conversion frequency (%) |
|---|---|---|---|---|---|---|
| 0 | 60 | 2 | 3.3 | 0 | 0 | 0 |
| 1 | 60 | 21 | 35 | 4 | 19.0 | 0 |
| 2 | 60 | 49 | 81.7 | 23 | 46.9 | 21.73 |
| 3 | 60 | 39 | 65 | 11 | 28.2 | 9.1 |
| 4 | 60 | 11 | 18.3 | 1 | 9.1 | 0 |
表3 预培养时长对外植体愈伤组织诱导与分化的影响
Table 3 Effects of pre culture duration on the induction and differentiation of callus tissue in explants
预培养时间 Pre cultivation time (d) | 外植体数 Number of explants | 愈伤数 Number of callus | 愈伤形成率 Callus formation rate (%) | 再生芽数 Number of regenerated buds | 出苗率 Seedling emergence rate (%) | 转化频率 Conversion frequency (%) |
|---|---|---|---|---|---|---|
| 0 | 60 | 2 | 3.3 | 0 | 0 | 0 |
| 1 | 60 | 21 | 35 | 4 | 19.0 | 0 |
| 2 | 60 | 49 | 81.7 | 23 | 46.9 | 21.73 |
| 3 | 60 | 39 | 65 | 11 | 28.2 | 9.1 |
| 4 | 60 | 11 | 18.3 | 1 | 9.1 | 0 |
处理 Treatment | 外植体数 Number of explants | 愈伤数 Number of callus | 愈伤形成率 Callus formation rate (%) | 愈伤组织形态 Morphology of callus tissue |
|---|---|---|---|---|
| C1 | 60 | 27 | 45 | 白色须状物 |
| C2 | 60 | 51 | 85 | 鲜绿色、结构紧密 |
| C3 | 60 | 40 | 66.7 | 黄绿色,结构松散 |
| C4 | 60 | 30 | 50 | 白色须状物、结构松散 |
表4 外植体茎段愈伤组织诱导培养基的筛选
Table 4 Selection of induction medium for stem segment callus of explants
处理 Treatment | 外植体数 Number of explants | 愈伤数 Number of callus | 愈伤形成率 Callus formation rate (%) | 愈伤组织形态 Morphology of callus tissue |
|---|---|---|---|---|
| C1 | 60 | 27 | 45 | 白色须状物 |
| C2 | 60 | 51 | 85 | 鲜绿色、结构紧密 |
| C3 | 60 | 40 | 66.7 | 黄绿色,结构松散 |
| C4 | 60 | 30 | 50 | 白色须状物、结构松散 |
卡那霉素浓度 Kanamycin concentration (mg/L) | 外植体数 Number of explants | 再生芽数 Number of regenerated buds | 出苗率 Seedling emergence rate (%) | 转化频率 Conversion frequency(%) |
|---|---|---|---|---|
| 0 | 60 | 54 | 90 | 3.7 |
| 25 | 60 | 48 | 80 | 6.3 |
| 50 | 60 | 31 | 51.7 | 23.53 |
| 75 | 60 | 17 | 28.3 | 17.7 |
| 100 | 60 | 0 | 0 | 0 |
表5 不同卡那霉素浓度对植株再生的影响
Table 5 Effects of different kanamycin concentrations on plant regeneration
卡那霉素浓度 Kanamycin concentration (mg/L) | 外植体数 Number of explants | 再生芽数 Number of regenerated buds | 出苗率 Seedling emergence rate (%) | 转化频率 Conversion frequency(%) |
|---|---|---|---|---|
| 0 | 60 | 54 | 90 | 3.7 |
| 25 | 60 | 48 | 80 | 6.3 |
| 50 | 60 | 31 | 51.7 | 23.53 |
| 75 | 60 | 17 | 28.3 | 17.7 |
| 100 | 60 | 0 | 0 | 0 |
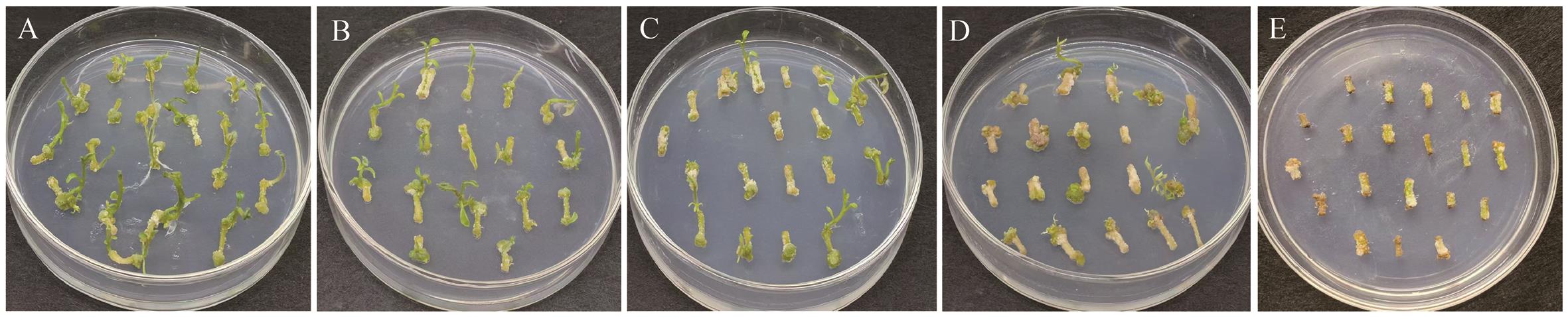
图4 不同卡那霉素浓度对再生植株的影响A-E表示卡那霉素浓度为0、25、50、75、100 mg/L
Fig. 4 Effects of different concentrations of kanamycin on regenerated plantsA-E refers to kanamycin concentrations of 0, 25, 50, 75, 100 mg/L, respectively
卡那霉素浓度 Kanamycin concentration (mg/L) | 外植体数 Number of explants | 生根外植体数 Number of rooting explants | 生根率 Rooting rate (%) |
|---|---|---|---|
| 0 | 40 | 40 | 100 |
| 50 | 40 | 40 | 100 |
| 75 | 40 | 0 | 0 |
| 100 | 40 | 0 | 0 |
表6 不同卡那霉素浓度对植株生根的影响
Table 6 Effects of different kanamycin concentrations on plant rooting
卡那霉素浓度 Kanamycin concentration (mg/L) | 外植体数 Number of explants | 生根外植体数 Number of rooting explants | 生根率 Rooting rate (%) |
|---|---|---|---|
| 0 | 40 | 40 | 100 |
| 50 | 40 | 40 | 100 |
| 75 | 40 | 0 | 0 |
| 100 | 40 | 0 | 0 |

图5 不同卡那霉素浓度对植株生根的影响A-D表示卡那霉素浓度为0、50、75、100 mg/L,E表示转基因植株在75 mg/L卡那霉素浓度下的生根状态
Fig. 5 Effects of different concentrations of kanamycin on plant rootingA-D indicate kanamycin concentrations of 0, 50, 75, and 100 mg/L, respectively, while E refers to the rooting status of transgenic plants under a 75 mg/L kanamycin concentration
处理 Treatment | 羧苄青霉素浓度 Carbenicillin concentration (mg/L) | 特美汀浓度 Timentin concentration (mg/L) | 诱导愈伤培养 Induced callus culture | 诱导出芽培养 Induced budding culture | 生根培养 Rooting culture |
|---|---|---|---|---|---|
| 1 | 100 | 0 | 染菌 | 染菌 | 染菌 |
| 2 | 200 | 0 | 染菌 | 染菌 | 染菌 |
| 3 | 300 | 0 | 染菌 | 染菌 | 染菌 |
| 4 | 0 | 100 | 染菌 | 染菌 | 染菌 |
| 5 | 0 | 200 | 未染菌 | 未染菌 | 未染菌 |
| 6 | 0 | 300 | 未染菌 | 未染菌 | 未染菌 |
表7 不同抑菌剂的种类及浓度对转化的影响
Table 7 Effects of different types and concentrations of antibacterial agents on conversion
处理 Treatment | 羧苄青霉素浓度 Carbenicillin concentration (mg/L) | 特美汀浓度 Timentin concentration (mg/L) | 诱导愈伤培养 Induced callus culture | 诱导出芽培养 Induced budding culture | 生根培养 Rooting culture |
|---|---|---|---|---|---|
| 1 | 100 | 0 | 染菌 | 染菌 | 染菌 |
| 2 | 200 | 0 | 染菌 | 染菌 | 染菌 |
| 3 | 300 | 0 | 染菌 | 染菌 | 染菌 |
| 4 | 0 | 100 | 染菌 | 染菌 | 染菌 |
| 5 | 0 | 200 | 未染菌 | 未染菌 | 未染菌 |
| 6 | 0 | 300 | 未染菌 | 未染菌 | 未染菌 |
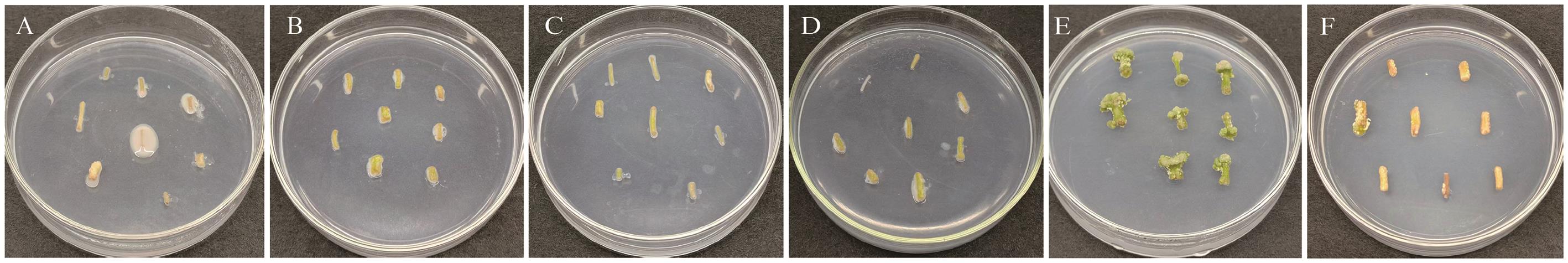
图6 不同抑菌剂的种类及浓度对转化的影响A-C表示羧苄青霉素浓度为100、200、300 mg/L,D-F表示特美汀浓度为100、200、300 mg/L
Fig. 6 Effects of different types and concentrations of antibacterial agents on conversionA-C refer to concentrations of carbenicillin at 100, 200, and 300 mg/L, while D-F refer to concentrations of timentin at 100, 200, and 300 mg/L
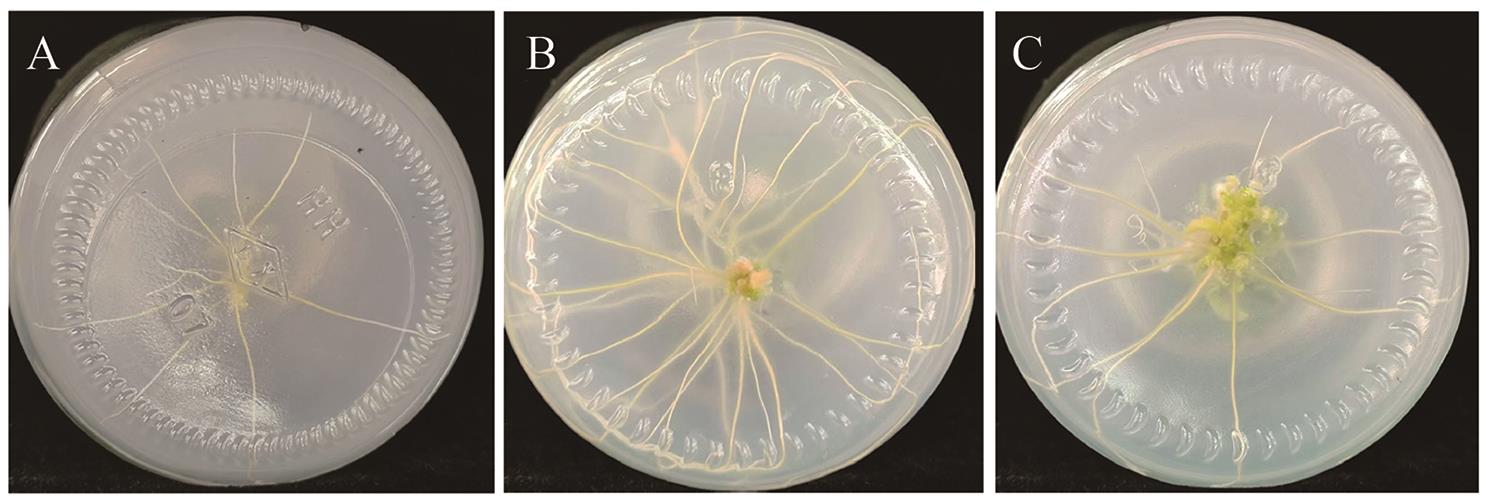
图7 不同浓度 IAA对转化植株根诱导及再生的影响A-C表示IAA浓度为0.2、0.6、1.2 mg/L
Fig. 7 Effects of different concentrations of IAA on the root induction and regeneration of transformed plantsA-C indicate IAA concentrations of 0.2, 0.6, and 1.2 mg/L
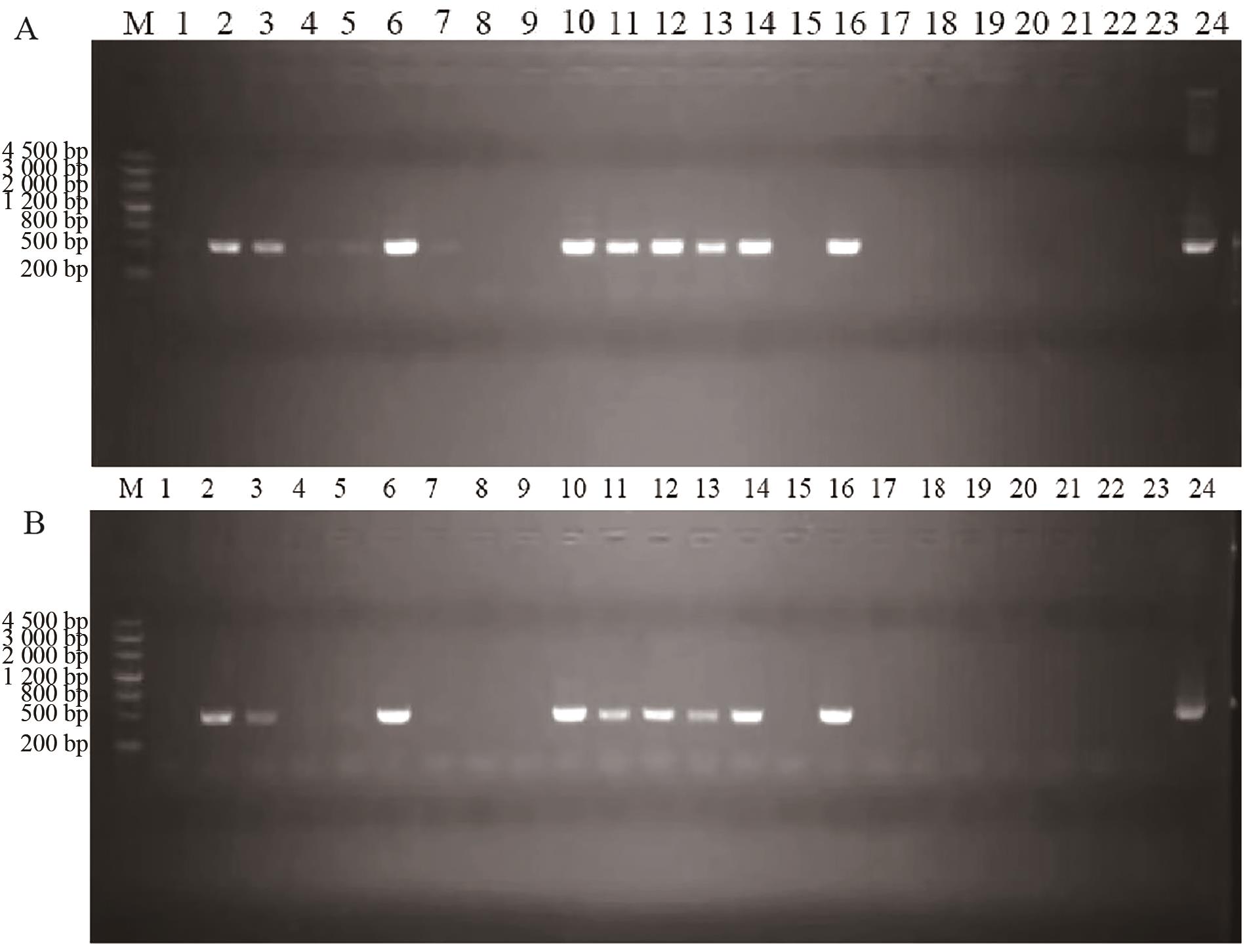
图8 再生植株的PCR阳性检测A:用引物CP-F,CP-R扩增的PCR产物,B:用引物CP-f,CP-r扩增的PCR产物。M:Marker;1-21:转化植株;22:阴性对照;23:空白对照;24:阳性对照
Fig. 8 PCR positive detection of regenerated plantsA: PCR products corresponding to primers CP-F and CP-R. B: PCR products corresponding to primers CP-f and CP-R. M: Marker; 1-21: transforming plants; 22: negative control; 23: blank control; 24: positive control
| [1] | Birch PRJ, Bryan G, Fenton B, et al. Crops that feed the world 8: Potato: are the trends of increased global production sustainable? [J]. Food Secur, 2012, 4(4): 477-508. |
| [2] | 朱雪瑞, 季静, 王罡, 等. 马铃薯不同组织的诱导分化及其对遗传转化效率的影响 [J]. 中国生物工程杂志, 2016, 36(10): 53-59. |
| Zhu XR, Ji J, Wang G, et al. Influence on the conversion efficiency of induced differentiation of various potato tissues [J]. China Biotechnol, 2016, 36(10): 53-59. | |
| [3] | Zhou Q, Tang D, Huang W, et al. Haplotype-resolved genome analyses of a heterozygous diploid potato [J]. Nat Genet, 2020, 52(10): 1018-1023. |
| [4] | 文博霖, 万敏, 胡建军, 等. 马铃薯川芋50遗传转化及基因编辑体系的建立 [J]. 生物技术通报, 2025, 41(4): 88-97. |
| Wen BL, Wan M, Hu JJ, et al. Establishment of genetic transformation and gene editing system for a potato cultivar Chuanyu 50 [J]. Biotechnol Bull, 2025, 41(4): 88-97. | |
| [5] | 张贵合, 郭华春. PVY和PVS病毒复合侵染对马铃薯光合及营养品质的影响 [J]. 西北植物学报, 2017, 37(8): 1569-1576. |
| Zhang GH, Guo HC. Variation of photosynthesis and nutritional quality of potato after infection with PVY and PVS complex virus [J]. Acta Bot Boreali Occidentalia Sin, 2017, 37(8): 1569-1576. | |
| [6] | 王拴福. 马铃薯退化与脱毒种薯应用 [J]. 种子, 2014, 33(2): 125-126. |
| Wang SF. Potato degeneration and the application of virus-free potato seed [J]. Seed, 2014, 33(2): 125-126. | |
| [7] | Gao FL, Kawakubo S, Ho SYW, et al. The evolutionary history and global spatio-temporal dynamics of potato virus Y [J]. Virus Evol, 2020, 6(2): veaa056. |
| [8] | 蔡一鸣. MSH1 RNAi干扰载体的构建及转基因芥菜的获得 [D]. 重庆: 西南大学, 2014. |
| Cai YM. Construction of MSH1 RNAi expression vector and its transformation to Brassica juncea [D]. Chongqing: Southwest University, 2014. | |
| [9] | 李奇科, 陶刚, 邱又彬, 等. 马铃薯Y病毒CP基因RNAi载体构建与干涉效果测定 [J]. 基因组学与应用生物学, 2009, 28(3): 460-464. |
| Li QK, Tao G, Qiu YB, et al. RNAi vector targeting and interference effect determination of PVY CP gene [J]. Genom Appl Biol, 2009, 28(3): 460-464. | |
| [10] | 姜芳. 马铃薯Y病毒CP基因不同区段对发夹RNA和人工的miRNA介导的病毒抗性的影响 [D]. 泰安: 山东农业大学, 2011. |
| Jiang F. Special origin of PVY CP influences the resistance of hairpin RNA and artificial miRNA expressing plants against PVY [D]. Tai’an: Shandong Agricultural University, 2011. | |
| [11] | 齐恩芳, 贾小霞, 刘石, 等. 利用RNA干扰介导抗病性获得兼抗四种病毒的转基因马铃薯 [J]. 植物保护学报, 2019, 46(1): 192-200. |
| Qi EF, Jia XX, Liu S, et al. Production of transgenic potato plants resistant to four viruses via RNAi-mediated virus resistance [J]. J Plant Prot, 2019, 46(1): 192-200. | |
| [12] | 李楠楠, 左玉玲, 隋炯明, 等. 重组CP多克隆抗体在马铃薯卷叶病毒DAS-ELISA检测中的应用 [J]. 华北农学报, 2011, 26(6): 85-88. |
| Li NN, Zuo YL, Sui JM, et al. Application of polyclonal antibody against the recombinant CP to the DAS-ELISA detection of potato leafroll virus [J]. Acta Agric Boreali Sin, 2011, 26(6): 85-88. | |
| [13] | 康霞, 徐刚, 王玉萍. 根癌农杆菌(Agrobacterium tume faciens)介导的马铃薯高效遗传转化体系筛选及优化 [J]. 中国沙漠, 2016, 36(1): 225-231. |
| Kang X, Xu G, Wang YP. Screening and optimization Agrobacterium tume faciens mediated potato genetic transformation system [J]. J Desert Res, 2016, 36(1): 225-231. | |
| [14] | 罗源. 马铃薯再生体系的建立及HAL1基因遗传转化研究 [D]. 杨凌: 西北农林科技大学, 2007. |
| Luo Y. Establishment of efficient regeneration system of potato and transformation of HAL1 gene [D]. Yangling: Northwest A & F University, 2007. | |
| [15] | 鲍红春, 李小雷, 王建平, 等. 马铃薯品种陇薯5号茎段再生体系的建立 [J]. 内蒙古农业科技, 2014, 42(2): 31-32. |
| Bao HC, Li XL, Wang JP, et al. Establishment of regeneration system for potato variety longshu No.5 [J]. Inn Mong Agric Sci Technol, 2014, 42(2): 31-32. | |
| [16] | 康哲秀, 吴京姬, 郎贤波, 等. 马铃薯延薯4号再生体系建立 [J]. 黑龙江农业科学, 2016(12): 11-13. |
| Kang ZX, Wu JJ, Lang XB, et al. Establishment of the regeneration system of potato variety Yanshu 4 [J]. Heilongjiang Agric Sci, 2016(12): 11-13. | |
| [17] | 牛瑜琦. 马铃薯晋薯16号再生体系建立及遗传转化研究 [D]. 太原: 山西大学, 2021. |
| Niu YQ. Establishment of regeneration system and genetic transformation of potato Jinshu 16 [D]. Taiyuan: Shanxi University, 2021. | |
| [18] | 李晶. 马铃薯再生体系的建立及遗传转化的研究 [D]. 哈尔滨: 东北农业大学, 2003. |
| Li J. Establishment of the regeneration system and study for the genetic transformation of potato [D]. Harbin: Northeast Agricultural University, 2003. | |
| [19] | 王清, 王蒂, 戴朝曦, 等. 奈乙酸、2, 4-D对马铃薯愈伤组织细胞染色体倍性的影响 [J]. 甘肃农业大学学报, 1997, 32(4): 304-307. |
| Wang Q, Wang D, Dai ZX, et al. Effect of NAA and 2,4-D and their concentrations on chromosomeploidy of potato calli in vitro culture [J]. J Gansu Agric Univ, 1997, 32(4): 304-307. | |
| [20] | 杨明贺, 朱旭, 李楠, 等. 马铃薯茎段高频再生体系的建立 [J]. 东北农业科学, 2019, 44(1): 57-62. |
| Yang MH, Zhu X, Li N, et al. Establishment of stem-based high-frequency regeneration procedure for potato [J]. J Northeast Agric Sci, 2019, 44(1): 57-62. | |
| [21] | 王萍, 王罡, 季静. 马铃薯两个基因型不同外植体的组织培养与植株再生 [J]. 中国马铃薯, 2006, 20(6): 326-328. |
| Wang P, Wang G, Ji J. Tissue culture and plant regeneration of various explants of two potato genotypes [J]. Chin Potato J, 2006, 20(6): 326-328. | |
| [22] | 程永芳, 张丽, 宋玉霞. 马铃薯高效遗传转化受体体系的建立 [J]. 西北农业学报, 2016, 25(9): 1350-1357. |
| Cheng YF, Zhang L, Song YX. Establishment of receptor system of high efficient genetic transformation in Solanum tuberosum L [J]. Acta Agric Boreali Occidentalis Sin, 2016, 25(9): 1350-1357. | |
| [23] | 杨春, 王桂梅. 愈伤组织再生马铃薯脱毒苗生产体系的建立 [J]. 中国马铃薯, 2008, 22(3): 137-139. |
| Yang C, Wang GM. Establishment of production system for regenerated virus-free potato plantlets through callus tissue [J]. Chin Potato J, 2008, 22(3): 137-139. | |
| [24] | 熊伟, 马耀华, 胡碧波, 等. 根癌农杆菌介导的马铃薯转化系统的优化 [J]. 广西农业生物科学, 2007, 26(1): 1-7. |
| Xiong W, Ma YH, Hu BB, et al. Optimized Agrobacterium-mediated transformation system for potato [J]. J Guangxi Agric Biol Sci, 2007, 26(1): 1-7. | |
| [25] | 叶明旺, 张春芝, 黄三文. 二倍体栽培马铃薯高效遗传转化体系的建立 [J]. 中国农业科学, 2018, 51(17): 3249-3257. |
| Ye MW, Zhang CZ, Huang SW. Construction of high efficient genetic transformation system for diploid potatoes [J]. Sci Agric Sin, 2018, 51(17): 3249-3257. | |
| [26] | 张西英, 张爱萍, 刘江娜. 马铃薯遗传转化体系的优化建立及其主要影响因素 [J]. 基因组学与应用生物学, 2019, 38(7): 3174-3179. |
| Zhang XY, Zhang AP, Liu JN. Optimization establishment of the genetic transformation system of potato and its main influencing factors [J]. Genom Appl Biol, 2019, 38(7): 3174-3179. | |
| [27] | 张丽, 宋玉霞, 巩檑, 等. 农杆菌介导的马铃薯转化研究进展 [J]. 分子植物育种, 2015, 13(7): 1660-1667. |
| Zhang L, Song YX, Gong L, et al. Progress on genetic transformation of potato mediated by Agrobacterium [J]. Mol Plant Breed, 2015, 13(7): 1660-1667. | |
| [28] | 宋倩娜, 梅超, 霍利光, 等. 马铃薯品种‘并薯6号’遗传转化体系的建立 [J]. 中国马铃薯, 2021, 35(5): 385-396. |
| Song QN, Mei C, Huo LG, et al. Establishment of genetic transformation system for potato variety ‘Bingshu 6’ [J]. Chin Potato J, 2021, 35(5): 385-396. | |
| [29] | 蒋继滨, 高冬丽, 朱曦鉴, 等. 二倍体马铃薯基因编辑载体快速验证体系的建立 [J]. 种子, 2019, 38(10): 29-33. |
| Jiang JB, Gao DL, Zhu XJ, et al. Establishment of a rapid verification system for diploid potato gene editing vector [J]. Seed, 2019, 38(10): 29-33. | |
| [30] | 杨亚萍, 李永兰, 梁月荣, 等. 发根农杆菌抑菌剂的抑菌效果及对茶组培苗丛生芽的影响 [J]. 茶叶科学, 2015, 35(5): 437-441, 442. |
| Yang YP, Li YL, Liang YR, et al. Antibiotics inhibition to Agrobaceterium rhizogenes and effect to tea multiple shoots [J]. J Tea Sci, 2015, 35(5): 437-441, 442. | |
| [31] | 王芳, 姜静. 不同抗生素对紫雨桦离体叶片愈伤组织诱导的影响 [J]. 西南林业大学学报, 2014(3): 27-31. |
| Wang F, Jiang J. Effects of different antibiotics on induction of callus from the leaves of Betula pendula ‘purple rain’ [J]. J Southwest For Univ, 2014(3): 27-31. | |
| [32] | 牛颜冰, 郭失迷, 宋艳波, 等. RNA沉默-新型的植物病毒病害防治策略 [J]. 中国生态农业学报, 2005, 13(2): 47-50. |
| Niu YB, Guo SM, Song YB, et al. RNA silencing-a new strategy for the control of virus diseases in plants [J]. Chin J Eco Agric, 2005, 13(2): 47-50. | |
| [33] | 赵爽, 王琦, 李艳红. 植物病毒诱导的基因沉默效应的分子机制 [J]. 植物生理学通讯, 2007, 43(2): 384-390. |
| Zhao S, Wang Q, Li YH. Molecular mechanism of virus induced gene silencing in plants [J]. Plant Physiol Commun, 2007, 43(2): 384-390. | |
| [34] | Wang MB, Abbott DC, Waterhouse PM. A single copy of a virus-derived transgene encoding hairpin RNA gives immunity to barley yellow dwarf virus [J]. Mol Plant Pathol, 2000, 1(6): 347-356. |
| [1] | 陈静欢, 房国楠, 朱文豪, 叶广继, 苏旺, 贺苗苗, 杨生龙, 周云. 马铃薯种质资源淀粉表征及相关基因表达分析[J]. 生物技术通报, 2026, 42(1): 170-183. |
| [2] | 巩慧玲, 邢玉洁, 马俊贤, 蔡霞, 冯再平. 马铃薯LAC基因家族的鉴定及盐胁迫下表达分析[J]. 生物技术通报, 2025, 41(9): 82-93. |
| [3] | 卢瑶, 袁平平, 金鑫, 毛向红, 范向斌, 白小东. 基于SSR标记的马铃薯野生种和地方种遗传多样性分析和指纹图谱构建[J]. 生物技术通报, 2025, 41(9): 94-104. |
| [4] | 黄丹丹, 吴云翼, 邹建华, 俞婷, 朱炎辉, 杨梅宏, 董文丽, 高冬丽. 马铃薯StPTST2a基因的克隆及互作分析[J]. 生物技术通报, 2025, 41(7): 172-180. |
| [5] | 李霞, 张泽伟, 刘泽军, 王楠, 郭江波, 辛翠花, 张彤, 简磊. 马铃薯转录因子StMYB96的克隆及功能研究[J]. 生物技术通报, 2025, 41(7): 181-192. |
| [6] | 罗稷林, 栗锦烨, 贾玉鑫. 马铃薯中重力响应调节基因鉴定及功能分析[J]. 生物技术通报, 2025, 41(6): 109-118. |
| [7] | 许慧珍, SHANTWANA Ghimire, RAJU Kharel, 岳云, 司怀军, 唐勋. 马铃薯SUMO E3连接酶基因家族分析及StSIZ1基因的克隆与表达模式分析[J]. 生物技术通报, 2025, 41(6): 119-129. |
| [8] | 段永红, 杨欣, 于冠群, 夏俊俊, 宋陆帅, 白小东, 彭锁堂. 125份马铃薯种质资源遗传多样性及主成分分析[J]. 生物技术通报, 2025, 41(6): 130-143. |
| [9] | 宋慧洋, 苏宝杰, 李京昊, 梅超, 宋倩娜, 崔福柱, 冯瑞云. 马铃薯StAS2-15基因的克隆及盐胁迫下功能分析[J]. 生物技术通报, 2025, 41(5): 119-128. |
| [10] | 文博霖, 万敏, 胡建军, 王克秀, 景晟林, 王心悦, 朱博, 唐铭霞, 李兵, 何卫, 曾子贤. 马铃薯川芋50遗传转化及基因编辑体系的建立[J]. 生物技术通报, 2025, 41(4): 88-97. |
| [11] | 刘涛, 王志淇, 吴文博, 石文婷, 王超楠, 杜崇, 杨中敏. 马铃薯GRAM基因家族鉴定与表达分析[J]. 生物技术通报, 2025, 41(4): 145-155. |
| [12] | 张益瑄, 马宇, 王童童, 盛苏奥, 宋家凤, 吕钊彦, 朱晓彪, 侯华兰. 马铃薯DIR家族全基因组鉴定及表达模式分析[J]. 生物技术通报, 2025, 41(3): 123-136. |
| [13] | 俞婷, 黄丹丹, 朱炎辉, 杨梅宏, 艾菊, 高冬丽. 马铃薯Stpatatin 05基因转录调控因子筛选及互作验证[J]. 生物技术通报, 2025, 41(3): 137-145. |
| [14] | 覃悦, 杨妍, 张磊, 卢丽丽, 李先平, 蒋伟. 二倍体和四倍体马铃薯StGAox基因鉴定与比较分析[J]. 生物技术通报, 2025, 41(3): 146-160. |
| [15] | 罗明凯, 张豪杰, 石晖琴, 李亚楠, 封瑞超, 沈硕. 三株马铃薯炭疽病生防菌的分离鉴定及其高抑菌活性培养物发酵参数优化[J]. 生物技术通报, 2025, 41(12): 313-327. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||